La normativa de tecnovigilancia en Latinoamérica cambia según el país: Colombia exige reportar eventos serios en 72 horas (INVIMA), Ecuador en 48 horas (ARCSA) y otros países aplican criterios inmediatos.
Cumplir estos plazos exige trazabilidad digital y procesos automatizados que protejan la seguridad hospitalaria y eviten sanciones.
Un dispositivo médico falla en un quirófano. En ese preciso instante, además del protocolo clínico, el reloj comienza a correr de maneras muy distintas. Y ese reloj no corre igual en Bogotá, Quito o Buenos aires.
Como ingenieros clínicos sabemos que la seguridad hospitalaria no depende solo del mantenimiento preventivo. También depende de cumplir con la normativa de tecnovigilancia sin errores ni retrasos.
¿Qué es la tecnovigilancia y por qué cambia su regulación en cada país?
La tecnovigilancia es el sistema que permite identificar, evaluar y reportar incidentes o eventos adversos relacionados con dispositivos médicos después de su comercialización. Aunque todos los países tienen como objetivo proteger la seguridad hospitalaria y al paciente, cada uno ha desarrollado marcos regulatorios propios con diferentes niveles de exigencia.
En Colombia, el INVIMA para eventos adversos serios exige un tiempo de 72 horas; en Ecuador ARCSA establece 48 horas. México (COFEPRIS) clasifica por riesgo, y Argentina (ANMAT) exige lo urgente en el momento. Esto obliga a hospitales multinacionales a adoptar el estándar más duro.
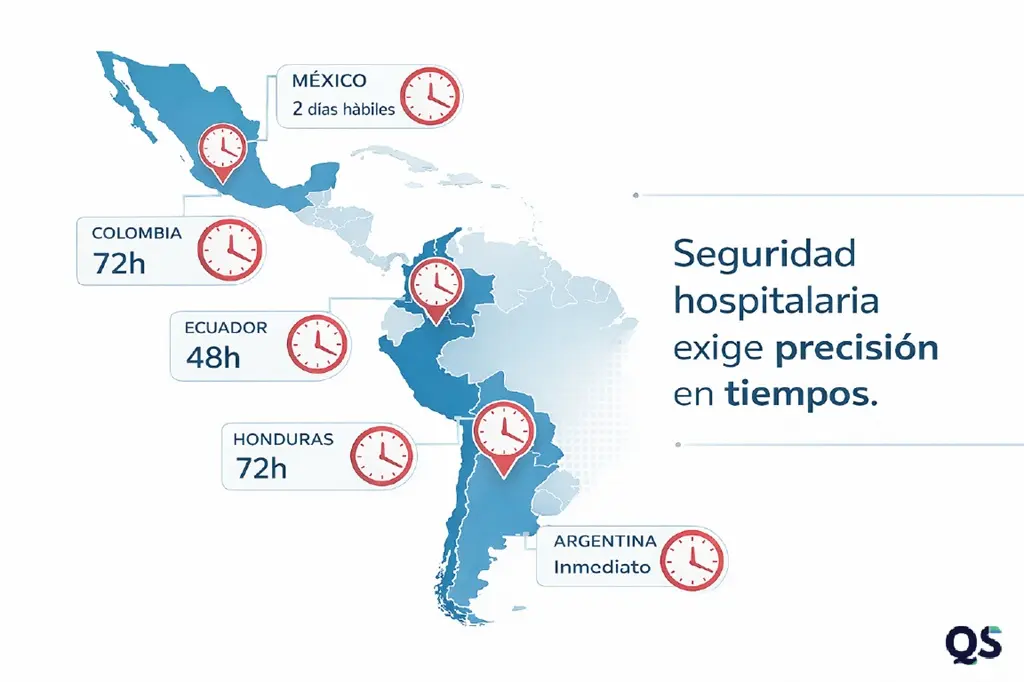
¿Cuáles son los plazos de reporte que impactan directamente la seguridad hospitalaria?
La diferencia más crítica está en el tiempo disponible para reportar un evento adverso serio. Colombia otorga 72 horas; Ecuador, 48 horas. Otros países exigen notificación inmediata. Esto obliga a los hospitales regionales a trabajar bajo un estándar más estricto si quieren evitar incumplimientos.
| País | Autoridad | Normativa Clave (Fuente) | Plazo Evento Serio (Dato Exacto) |
|---|---|---|---|
| Colombia | INVIMA | Res. 4816 de 2008 | 72 horas |
| Ecuador | ARCSA | Res. ARCSA-DE-2023-016 | 72 horas (Estándar) / 48h (Estricto) |
| Argentina | ANMAT | Disp. 8054/10 | Inmediato (Sin demora injustificada) |
| México | COFEPRIS | NOM-240-SSA1-2012 | 2 días hábiles |
| Honduras | ARSA | Regulación ARSA / RTCA | 72 horas |
Resumen visual de plazos de reporte
Gestionar esta matriz en una hoja de cálculo puede volverse complejo cuando los equipos crecen, las sedes se multiplican y los tiempos regulatorios se acortan. Aquí es donde puedes tener la tecnovigilancia a tu favor: contar con herramientas que centralizan la información es la clave para asegurar la seguridad del paciente y la continuidad del servicio.
¿Necesitas eliminar la complejidad de gestionar múltiples plazos manualmente?
Solicita una DEMO de QSystems hoy mismo y descubre cómo nuestro software automatiza las alertas regulatorias según el país de operación.
¿Cómo asegurar trazabilidad sin complicaciones en eventos adversos?
Garantizar trazabilidad significa poder reconstruir la historia completa de un equipo médico: desde adquisición, mantenimiento, fallas, incidentes hasta decisiones tomadas. Sin la trazabilidad digital, la tecnovigilancia se vuelve frágil en auditorías y en las buenas practicas de la ingeniería clínica.
En la práctica existen algunos pasos críticos:
-
Identificación correcta:
¿ El fallo fue del equipo o del uso? -
Control:
Implementación de planes de mejora (acciones correctivas y preventivas) -
Análisis:
Uso de herramientas como el diagrama de Ishikawa (espina de pescado), análisis de causa raíz o evaluación de uso vs falla técnica
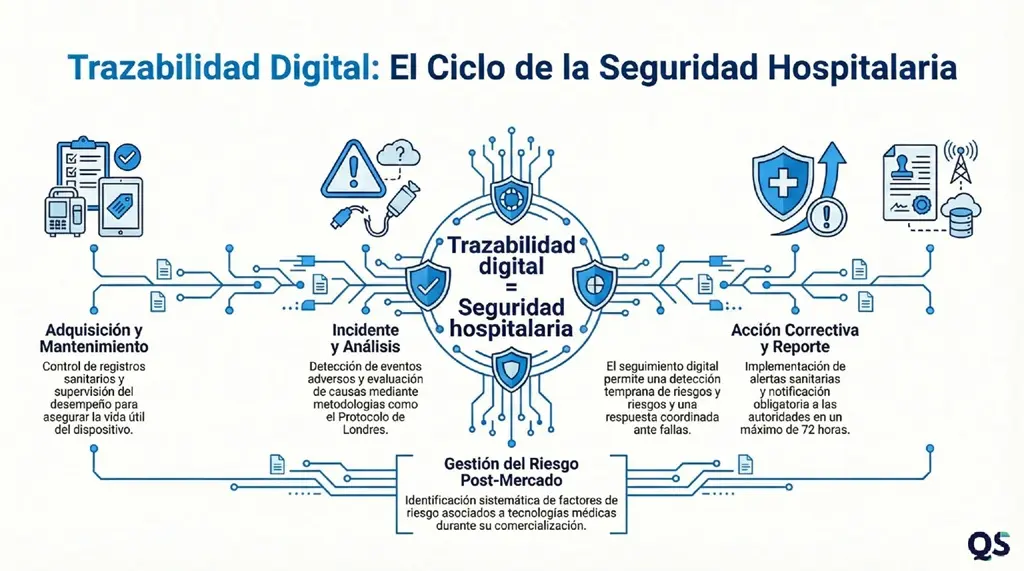
Un error muy común es reportar fallas de mantenimiento como eventos adversos regulatorios. Esto puede generar ruido estadístico y debilitar la credibilidad del programa. Para evitar este tipo de errores, es importante saber diferenciar cuando nos encontramos ante un problema de disponibilidad (mantenimiento) y cuándo ante uno de seguridad (tecnovigilancia), si la falla se detecta antes de tocar al paciente o no implica un riesgo real de daño, estamos gestionando activos, no vigilando riesgos.
¿Por qué la automatización es clave para cumplir la normativa de tecnovigilancia en Latinoamérica?
La automatización es el único camino viable porque elimina la variabilidad humana en el seguimiento de fechas, centraliza la hoja de vida del equipo en tiempo real y asegura la integridad de los datos ante cualquier auditoría .En un entorno donde la seguridad hospitalaria depende de tiempos precisos y datos verificables, confiar en procesos manuales ya no es suficiente.
Aquí es donde un CMMS especializado como QS actua a tu favor. Más allá de centralizar información, integra módulos de rondas técnicas, inventarios actualizados, gestión de contratos, programación de mantenimientos y capacitaciones del personal, todo conectado con la hoja de vida digital de cada equipo.
Cada intervención, cada hallazgo en campo, cada reporte y cada documento contractual queda trazado en tiempo real. Esa trazabilidad convierte la operación diaria en una estrategia de tecnovigilancia proactiva: no se trata solo de reaccionar ante un evento adverso, sino de anticiparlo, detectarlo oportunamente y documentarlo con evidencia sólida. Así, lo que antes era un requisito regulatorio aislado se transforma en un sistema continuo de control técnico que fortalece la gestión, la auditoría y, sobre todo, la seguridad hospitalaria.

¿Cómo la comunidad fortalece tu cumplimiento en seguridad hospitalaria?
La seguridad hospitalaria no se construye en aislamiento.Se fortalece cuando los ingenieros clínicos de la región compartimos experiencias reales, alertas regulatorias y decisiones técnicas que ya fueron probadas en campo. La inteligencia colectiva reduce errores y eleva el estándar de cumplimiento.
Por eso, en la Comunidad de Ingeniería Clínica creada por y para ingenieros, se comparten experiencias, noticias y buenas prácticas que ahorran horas en auditorías. Lo más valioso es que no es un espacio pasivo. Puedes participar en charlas, compartir casos, hacer preguntas técnicas y generar conexiones que realmente impactan tu gestión diaria.
Si hoy llegara una auditoría de tecnovigilancia a tu hospital, ¿te sentirías completamente tranquilo con tu trazabilidad y tiempos de respuesta?
Si la respuesta no es un sí rotundo, vale la pena dar el siguiente paso. Agenda un DEMO con QS y revisemos juntos cómo fortalecer tu cumplimiento normativo y tu modelo de seguridad hospitalaria.
Para resumir: Seguridad hospitalaria, lo que realmente está en juego
La normativa de tecnovigilancia en Latinoamérica puede parecer compleja, pero en el fondo todo gira alrededor de lo mismo: proteger la seguridad hospitalaria de forma real y sostenible. No se trata solo de cumplir plazos ante las entidades regulatorias, sino de asegurar que cada decisión técnica respalda la confianza que un paciente deposita en la tecnología que lo está tratando.
Cuando un equipo falla, lo que se pone en juego no es únicamente un indicador de gestión. Es la continuidad del servicio, la tranquilidad del equipo clínico y la reputación institucional. Por eso, depender de hojas de cálculo aisladas o de recordatorios informales ya no es suficiente. La seguridad hospitalaria hoy exige trazabilidad en tiempo real, criterios claros de clasificación de eventos y evidencia lista para una auditoría.
Ingeniería Clínica
Conecta con la Comunidad de Ingeniería Clínica en Latam y mantente actualizado con noticias, eventos y tendencias que están transformando la gestión tecnológica en salud. Una comunidad creada por QS, software biomédico en Colombia.

